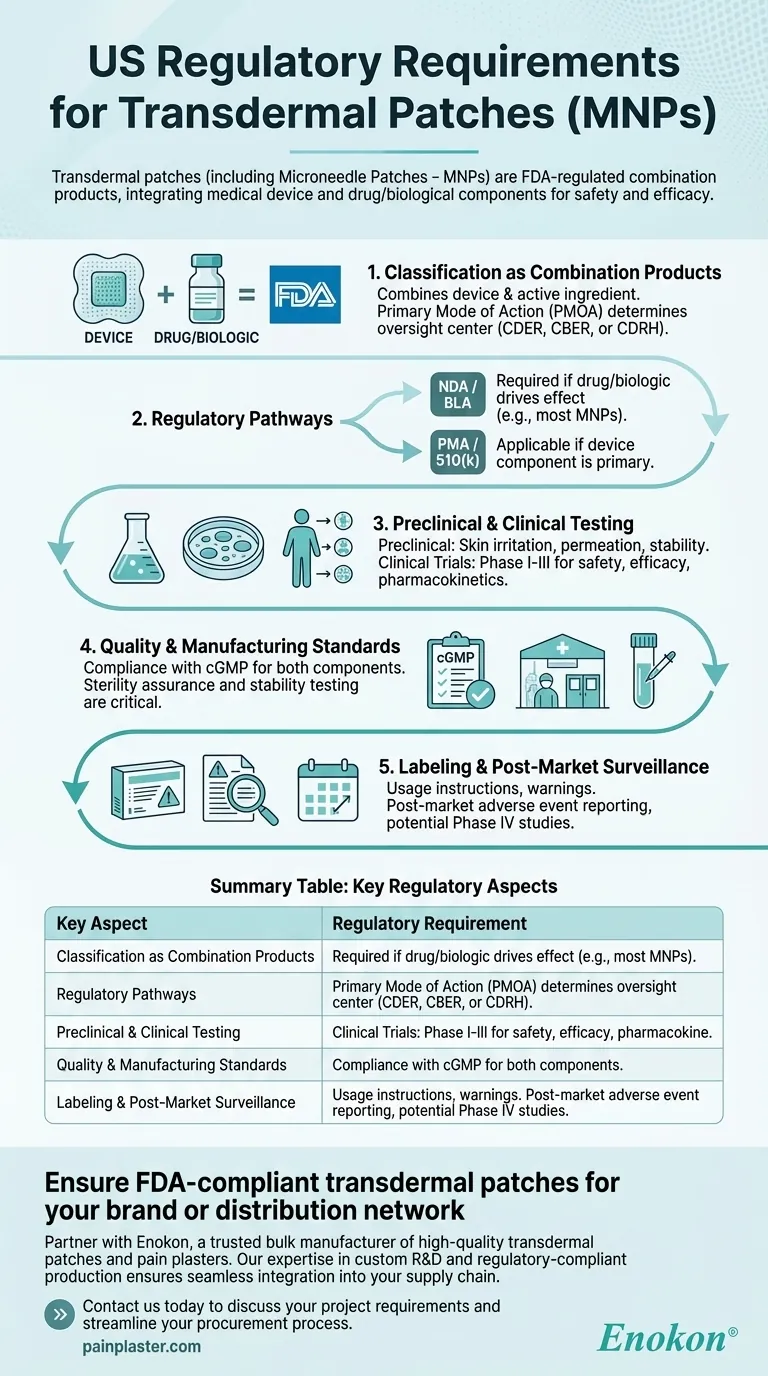
يتم تنظيم اللصقات عبر الجلد، بما في ذلك اللصقات ذات الإبر المجهرية (MNPs)، في الولايات المتحدة كمنتجات مركبة من قبل إدارة الغذاء والدواء الأمريكية، مما يتطلب عمليات موافقة صارمة لضمان السلامة والفعالية. تدمج هذه المنتجات بين مكونات الأجهزة الطبية والمكونات الدوائية/البيولوجية، مما يستلزم الامتثال لمسارات تنظيمية محددة اعتمادًا على طريقة عملها الأساسية. تتضمن عملية الموافقة اختبارات ما قبل السريرية والسريرية، ومراقبة الجودة، والالتزام بمعايير وضع العلامات ومعايير التصنيع.
شرح النقاط الرئيسية:
-
التصنيف كمنتجات مركبة
- تصنف إدارة الغذاء والدواء الأمريكية اللصقات عبر الجلد كمنتجات مركبة لأنها تجمع بين جهاز طبي (على سبيل المثال، دعامة اللصقة اللاصقة، الإبر المجهرية) مع دواء أو مكون نشط بيولوجي.
- يحدد أسلوب العمل الأساسي (PMOA) ما إذا كان المنتج خاضعًا للتنظيم من قبل مركز تقييم الأدوية والبحوث (CDER) أو مركز تقييم وبحوث البيولوجيا والبحوث (CBER) أو مركز الأجهزة والصحة الإشعاعية (CDRH).
-
المسارات التنظيمية
- طلب الحصول على دواء جديد (NDA) أو طلب ترخيص المستحضرات البيولوجية (BLA): مطلوب إذا كان الدواء أو المكون البيولوجي يؤدي إلى التأثير العلاجي.
- موافقة ما قبل التسويق (PMA) أو 510 (k): تنطبق إذا كان مكون الجهاز أساسيًا (مثل الإبر الدقيقة التي تسهل توصيل الدواء).
- وغالباً ما تتبع الإبر المجهرية متعددة البروتينات مسار NDA/BLA بسبب وظيفتها المتمحورة حول الدواء.
-
الاختبارات ما قبل السريرية والسريرية
- الدراسات ما قبل السريرية: تشمل اختبار تهيج الجلد والتخلل والثبات لتقييم السلامة وكفاءة التوصيل.
- التجارب السريرية: تجارب المرحلة الأولى إلى الثالثة لتقييم الحرائك الدوائية والفعالية والآثار الضارة على البشر.
-
معايير الجودة والتصنيع
- الامتثال لممارسات التصنيع الجيدة الحالية (cGMP) لكل من مكونات الدواء والجهاز.
- يعد ضمان العقم واختبار الثبات أمرًا بالغ الأهمية بالنسبة للبقع التي تحتوي على المستحضرات البيولوجية.
-
وضع الملصقات ومراقبة ما بعد السوق
- يجب أن تتضمن الملصقات تعليمات الاستخدام والتحذيرات وشروط التخزين.
- تشمل متطلبات ما بعد السوق الإبلاغ عن الأحداث العكسية ودراسات المرحلة الرابعة المحتملة.
بالنسبة للمشترين، يضمن فهم هذه المتطلبات للمشترين التوافق مع الموردين المتوافقين مع إدارة الغذاء والدواء، مما يقلل من مخاطر المنتجات غير المطابقة. هل فكرت في كيفية تأثير هذه اللوائح على الجداول الزمنية للمشتريات أو معايير اختيار الموردين؟ إن التفاعل بين الرقابة على الأجهزة والأدوية يشكل بهدوء موثوقية العلاجات الحديثة عبر الجلد.
جدول ملخص:
| الجانب الرئيسي | المتطلبات التنظيمية |
|---|---|
| التصنيف | يتم تنظيمها كمنتجات مركبة (جهاز + دواء/دواء/بيولوجي) من قبل إدارة الغذاء والدواء الأمريكية. |
| طريقة العمل الأساسية | تحدد الرقابة من قبل CDER (دواء) أو CBER (بيولوجي) أو CDRH (جهاز). |
| مسارات الموافقة | NDA/BLA (مدفوعة بالأدوية) أو PMA/510(k) (مدفوعة بالأجهزة). وعادةً ما تتبع مسارات الموافقة على الأدوية المتعددة الجنسيات مسارات الموافقة على الأدوية. |
| متطلبات الاختبار | التجارب قبل السريرية (السلامة والنفاذ) والتجارب السريرية (المراحل من الأولى إلى الثالثة). |
| معايير التصنيع | الامتثال لممارسات التصنيع الجيدة لكل من مكونات الأدوية والأجهزة؛ ضمان العقم للمواد البيولوجية. |
| التزامات ما بعد التسويق | الإبلاغ عن الأحداث الضارة، ودراسات المرحلة الرابعة، والامتثال لوضع العلامات. |
ضمان امتثال اللصقات عبر الجلد المتوافقة مع إدارة الأغذية والعقاقير لعلامتك التجارية أو شبكة التوزيع الخاصة بك
الشراكة مع
إنوكون
وهي شركة موثوق بها لتصنيع اللصقات عبر الجلد ولصقات الألم عالية الجودة عبر الجلد. تضمن خبرتنا في مجال البحث والتطوير المخصص والإنتاج المتوافق مع اللصاقات عبر الجلد المتوافقة مع اللوائح التنظيمية الاندماج السلس في سلسلة التوريد الخاصة بك.
اتصل بنا اليوم
لمناقشة متطلبات مشروعك وتبسيط عملية الشراء الخاصة بك.
دليل مرئي
المنتجات ذات الصلة
- لاصقة جل المنثول لتخفيف الآلام
- لاصقة دواء آيسي هوت منثول لتخفيف الألم
- لاصقات تسخين لتخفيف آلام الدورة الشهرية
- لاصقة الربو والسعال وتسكين الآلام للبالغين والأطفال
- لاصقة عشبية طبية مضادة للإسهال لتخفيف آلام الجهاز الهضمي
يسأل الناس أيضًا
- ما مدى فعالية لاصقات تخفيف الألم لآلام العضلات؟تخفيف مستهدف بدون آثار جانبية جهازية
- هل يمكن للمرأة الحامل استخدام لاصقات تخفيف الآلام؟شرح السلامة والبدائل
- كيف تقارن لصقات تخفيف الآلام بوسائل تخفيف الآلام الأخرى؟اكتشف الراحة المستهدفة طويلة الأمد
- ما هي الأنواع المختلفة من لاصقات تخفيف الألم المتاحة؟اعثر على الحل المناسب لألمك
- ما هي الآثار الجانبية المحتملة للاصقات تخفيف الألم؟المخاطر ونصائح السلامة